Erstattung von Medizinprodukten
- Strategische Beratung zur Erstattung von Medizinprodukten
- Erstellung von Anlage V-Anträgen
- Erstellung von Dossiers im Joint Clinical Assessment

Marktzugang und Erstattung von Medizinprodukten
Die Erstattung von Medizinprodukten in Deutschland unterscheidet sich fundamental von der Erstattung von Arzneimitteln: eine CE-Zertifizierung des Medizinprodukts bringt nicht eine grundsätzliche Erstattungsfähigkeit mit sich. Diese unterliegt unterschiedlichen Voraussetzungen, abhängig davon, ob das Medizinprodukt im ambulanten oder stationären Bereich eingesetzt wird, ob es mit einer neuen Methode verbunden ist oder nicht und welchem Medizinprodukttyp es entspricht.
Beispielsweise unterliegen die mit Medizinprodukten verbundenen ärztlichen Methoden im ambulanten Bereich dem sogenannten Erlaubnisvorbehalt: Sie sind erst dann erstattungsfähig, wenn der G-BA die Methode positiv bewertet hat. Im Gegenzug dazu gilt im stationären Bereich der Verbotsvorbehalt: Methoden dürfen so lange eingesetzt werden, bis der G-BA sie nach einer negativen Bewertung aus der Erstattung ausschließt.
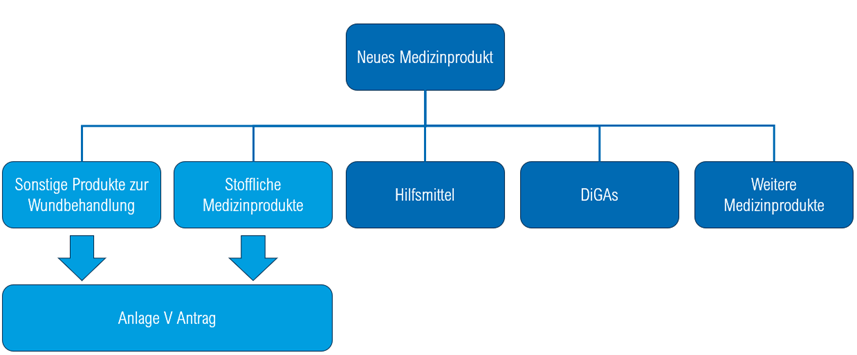
Abbildung 1: Übersicht über unterschiedliche Medizinproduktkategorien
Unsere Leistungen
Unsere Expertise besteht insbesondere in der Erstellung von Anlage V Anträgen für sonstige Produkte zur Wundbehandlung und stoffliche Medizinprodukte sowie in der Erstellung des Dossiers im Rahmen des Joint Clinical Assessments (JCA).
Erstellung von Anlage V Anträgen
In der Anlage V der Arzneimittel-Richtlinie (AM-RL) sind Medizinprodukte gelistet, die positiv bewertet wurden und deshalb zu Lasten der gesetzlichen Krankenversicherung (GKV) verordnungsfähig sind. Unter diese Regelung fallen sogenannte sonstige Produkte zur Wundbehandlung und stoffliche Medizinprodukte. Eine Aufnahme in diese Positivliste kann durch einen Anlage V Antrag beantragt werden. Hierfür muss der Medizinproduktehersteller mittels Studien von höchstmöglichem Evidenzniveau – idealerweise randomisiert kontrollierte Studien (RCT) – die Zweckmäßigkeit des Produkts, die medizinische Notwendigkeit und den therapeutischen Nutzen in der entsprechenden Patientenpopulation nachweisen. Nach einer Aufnahme in die Anlage V ist das Medizinprodukt nur für die Behandlung derjenigen Patientenpopulation erstattungsfähig, die Gegenstand der Bewertung waren.
Wundprodukte
Unter Wundprodukte fallen Verbandmittel und sonstige Produkte zur Wundbehandlung. Während Verbandmittel ihre Hauptwirkung über Bedecken, Aufsaugen, Stabilisieren, Immobilisieren oder Komprimieren entfalten, weisen sonstige Produkte zur Wundbehandlung eine über diese Eigenschaften hinausgehende therapeutische Wirkung auf. Sie können somit die Wundheilung durch eine pharmakologische, immunologische oder metabolische Wirkweise aktiv im menschlichen Körper beeinflussen.
Verbandmittel sind grundsätzlich unmittelbar erstattungsfähig. Sonstige Produkte zur Wundbehandlung hingegen müssen in die Anlage V der AM-RL aufgenommen werden und somit eine Bewertung durch den G-BA durchlaufen, um erstattungsfähig zu werden. Eine Ausnahme besteht für Produkte, die bereits vor dem 2. Dezember 2020 erstattungsfähig waren – diese sind im Rahmen einer mehrfach verlängerten gesetzlichen Übergangsregelung bis vorerst zum 31. Dezember 2026 erstattungsfähig.
Beispiele: Antimikrobielle Produkte zur Wundbehandlung (z. B. Silberhaltig, Honighaltig), Hydrogele oder Hydrokolloidverbände
Stoffliche Medizinprodukte
Stoffliche Medizinprodukte sind Substanzen oder Stoffzusammensetzungen, die Arzneimitteln in Aufmachung und Darreichung ähneln, im Gegensatz dazu aber primär physikalisch statt pharmakologisch, immunologisch oder metabolisch im menschlichen Körper wirken. Sie sind ebenfalls nicht unmittelbar erstattungsfähig. Auch für diese Produkte muss zunächst in einem Anlage V Antrag der therapeutische Nutzen im Rahmen von Studien höchstmöglicher Evidenz nachgewiesen werden.
Beispiele: Synthetische Tränenflüssigkeiten, bestimmte Spüllösungen bei operativen Eingriffen, Trägerlösungen bei der Verwendung von Inhalaten
Erstellung von Dossiers im JCA
Im Rahmen der Verordnung (EU) 2021/2282 können seit dem 12. Januar 2025 Medizinprodukte der Risikoklassen IIb und III sowie in-vitro-Diagnostika zur gemeinsamen klinischen Bewertung (Joint Clinical Assessment, JCA) herangezogen werden. Im Gegensatz zur sukzessiven Implementierung der JCAs bei Arzneimitteln zum Launch werden die betroffenen Medizinprodukte durch die Kommission nach Einholung einer Empfehlung der Koordinierungsgruppe ausgewählt.
Die Kriterien hierfür zielen vor allem auf den ungedeckten medizinischen Bedarf, mögliche Auswirkungen auf Patienten, öffentliche Gesundheit oder Gesundheitssysteme und darauf ab, ob es sich um das erste Produkt einer neuen Produktkategorie handelt. Folglich werden zunächst nur ausgewählte Medizinprodukte einem JCA-Prozess unterzogen. Dies resultiert in einer Planungsunsicherheit, da erst spät feststeht, ob für ein bestimmtes Produkt der JCA-Prozess durchlaufen werden muss. Nach Aufforderung muss der Medizinproduktehersteller ein Dossier mit höchstmöglicher Evidenz und potenziell Vergleichen gegenüber vielen PICOs vorlegen.
Weitere Kategorien von Medizinprodukten
Neben den o. g. gibt es unter anderem noch folgende Arten von Medizinprodukten:
Hilfsmittel
Hilfsmittel sind Produkte, die eine medizinische Behandlung unterstützen, Behinderungen ausgleichen oder einer drohenden Behinderung vorbeugen. Sie sind davon gekennzeichnet, dass sie in der Regel vom Patienten im häuslichen Gebrauch angewendet werden. Die erstattungsfähigen Hilfsmittel sind im Hilfsmittelverzeichnis des GKV-Spitzenverbandes gelistet.
Beispiele: Unterarmgehstützen, Prothesen, Atemhilfen, Rollstühle
Digitale Gesundheitsanwendungen (DiGA)
DiGAs sind Medizinprodukte auf App- oder Webbasis, welche von ärztlicher Seite verordnet werden. Sie werden deshalb auch als „Apps auf Rezept“ bezeichnet. Das BfArM bewertet den klinischen Nutzen und führt ein Verzeichnis über verordnungsfähige DiGAs.
Beispiele: Apps zur Behandlung von Rückenschmerzen, Angststörungen, Migräne oder Adipositas
Weitere Medizinprodukte
Darüber hinaus gibt es unterschiedlichste Medizinprodukte, deren Erstattung im Wesentlichen davon abhängt, ob sie im ambulanten oder stationären Bereich angewendet werden. Im ambulanten Bereich müssen Medizinprodukte, die Teil einer neuen Untersuchungs- oder Behandlungsmethode sind, eine Methodenbewertung nach § 135 SGB V durch den G-BA durchlaufen, um erstattungsfähig zu werden (Erlaubnisvorbehalt). Anschließend wird im Fall einer positiven Bewertung eine Abrechnungsziffer im Einheitlichen Bewertungsmaßstab (EBM) geschaffen. Im stationären Bereich werden Medizinprodukte grundsätzlich im Rahmen von den pauschalen DRGs erstattet, können aber im Rahmen einer Methodenbewertung nach § 137c SGB V vom G-BA verboten werden (Verbotsvorbehalt).
Beispiele: in-vitro-Diagnostika (Laboruntersuchungen), Geräte für bildgebende Diagnostik (z. B. MRT-Geräte) oder Produkte zur operativen Anwendung (z. B. Herzkatheter)
