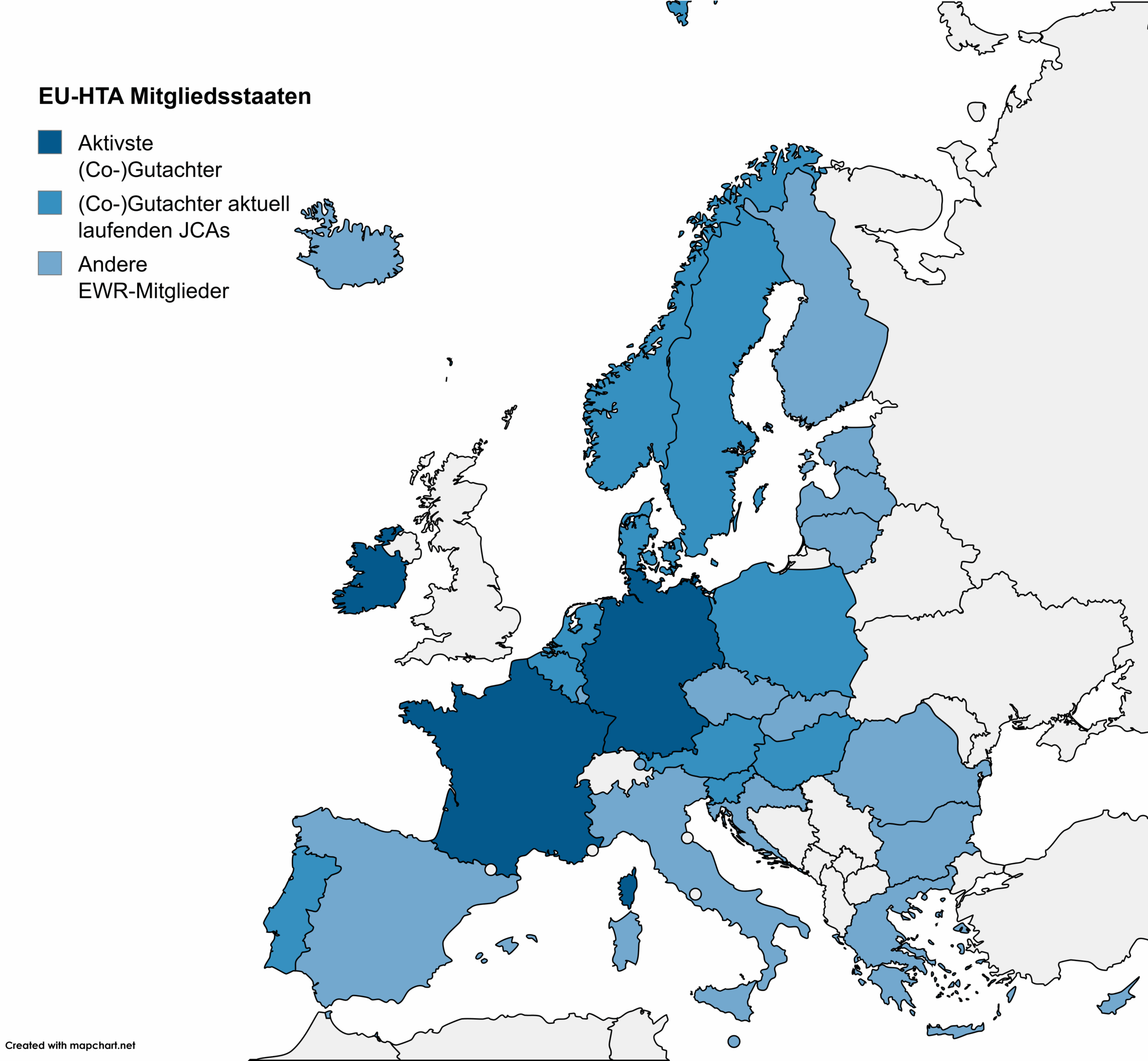
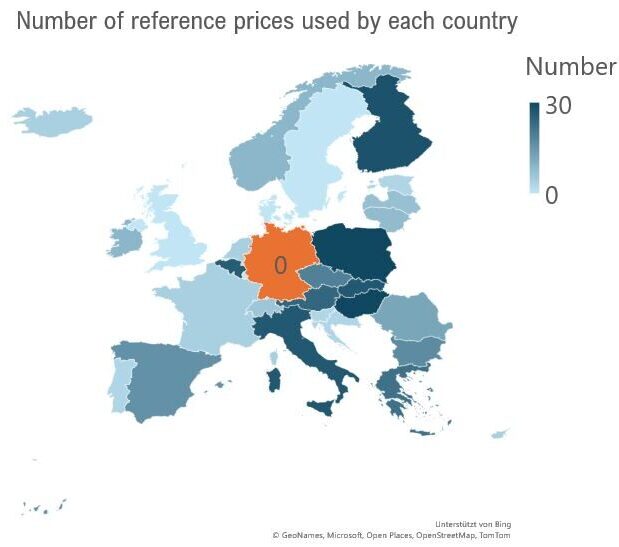
Für Produkte mit erstmaliger Markteinführung nach dem 1. Januar 2025 gelten nun weniger strenge Richtlinien zur Preisbildung (AMNOG Leitplanken), wenn die für die AMNOG-Nutzenbewertung herangezogenen Studien ≥ 5 % deutsche Patienten eingeschlossen haben. Dieser Vorteil gilt für drei Jahre nach Vereinbarung des Erstattungsbetrages und kann für Unternehmen mit aktiver Forschung in Deutschland auch danach beibehalten werden.
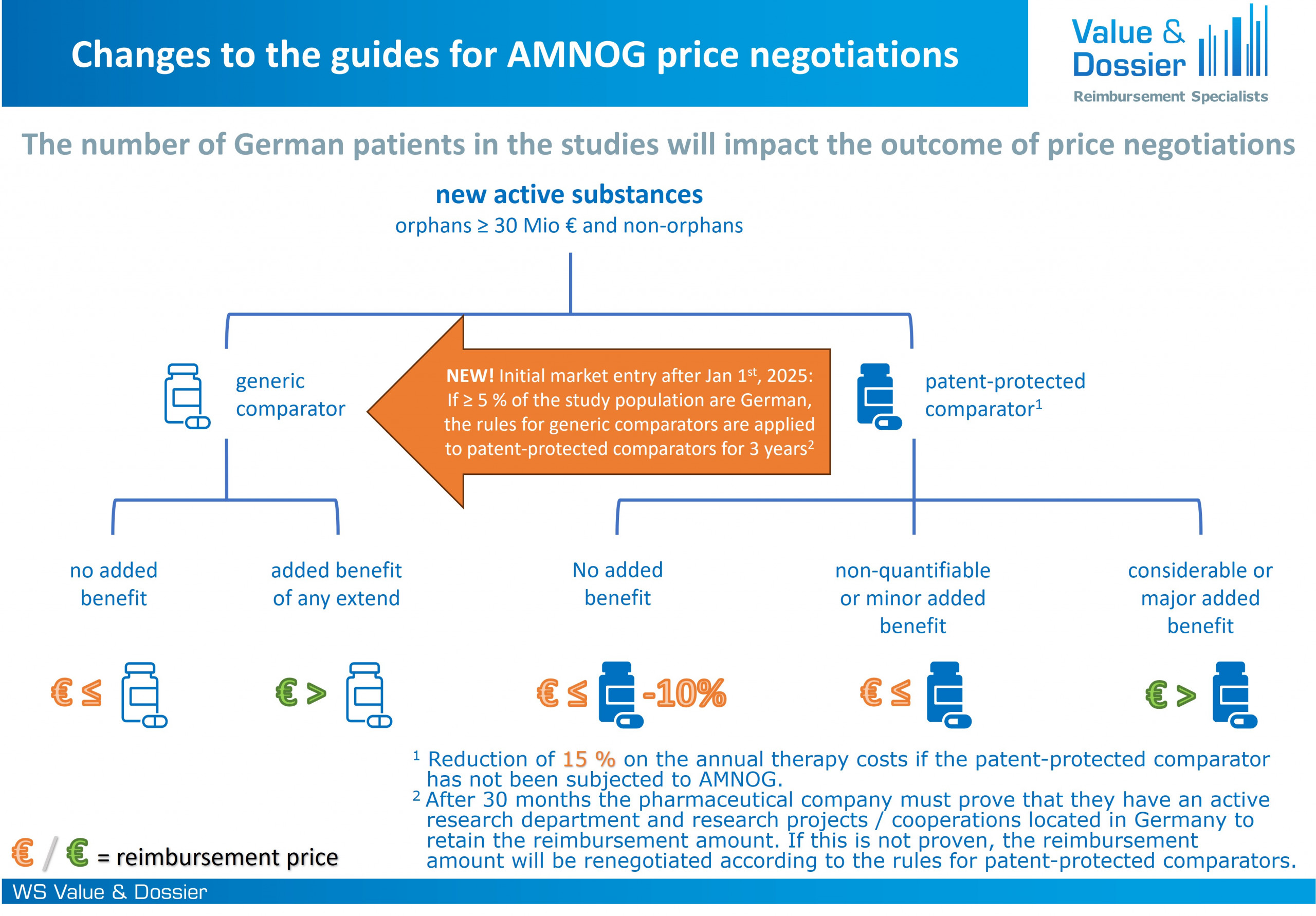
Abbildung 1: Die AMNOG-Leitplanken zählen nicht für neue Arzneimittel mit ≥ 5 % deutschen Patienten in der Studienpopulation.
Im November 2022 ist das GKV-Finanzstabilisierungsgesetz (GKV-FinStG) in Kraft getreten, in dem u. a. die sogenannten AMNOG-Leitplanken für die Verhandlungen zu den Erstattungsbeträgen von Arzneimitteln eingeführt worden sind. Mit diesen Regelungen wurden die gesetzlichen Vorgaben der Verhandlungen für die pharmazeutischen Unternehmen verschärft. Mit dem Medizinforschungsgesetz (MFG) werden die Arzneimittel von einzelnen Regelungen der AMNOG Leitplanken ausgenommen, bei denen ≥ 5 % deutsche Patienten in den bewertungsrelevanten, klinischen Studien eingeschlossen waren. Der auf den angepassten Regelungen basierende, potenziell höher vereinbarte Erstattungsbetrag ist 3 Jahre lang gültig. Betreibt ein pharmazeutisches Unternehmen eine aktive Forschung in Deutschland, kann der vereinbarte Erstattungsbetrag auch nach diesen 3 Jahren beibehalten werden. Die Anforderungen an eine aktive Forschung zielen darauf ab, den Forschungsstandort Deutschland zu stärken. Die erste Voraussetzung ist, dass das pharmazeutische Unternehmen eine permanente und aktive Forschungsabteilung in Deutschland vorweisen kann. Im Falle von Entwicklungskooperationen, Lizenzierungen oder Asset Deals ist es auch akzeptabel, wenn die Forschungsabteilung zum jeweiligen Kooperations- oder Lizenzpartner gehört. Darüber hinaus verlangt die zweite Bedingung, dass das pharmazeutische Unternehmen relevante eigene Projekte (z. B. gesponserte Studien) und/oder Kooperationen mit öffentlichen Forschungseinrichtungen in Deutschland unterhält. Die Projekte bzw. Kooperationen müssen laufend sein, abgeschlossene Projekte bzw. Kooperationen werden nicht akzeptiert. Pharmazeutische Unternehmen, die keine Forschungstätigkeit in Deutschland ausüben, sind verpflichtet, den Erstattungsbetrag nach Ablauf des Dreijahreszeitraums gemäß den strengen AMNOG-Leitplanken für patentgeschützte Komparatoren neu zu verhandeln.
Zusammengefasst sind Arzneimittel für die Dauer von 3 Jahren von den strengen AMNOG-Leitplanken des GKV-FinStG ausgenommen, wenn die für die AMNOG-Bewertung herangezogenen Studien ≥ 5 % deutsche Patienten umfassten. Dieser Vorteil kann auch nach diesen 3 Jahren beibehalten werden, wenn sich das pharmazeutische Unternehmen aktiv an der Forschung in Deutschland beteiligt. Da die Ergebnisse der Nutzenbewertung und der Preisverhandlungen maßgeblich von vielen anderen Faktoren abhängig ist, stellt sich die Frage, ob diese Anreize alleine ausreichend sind, Forschungsinvestitionen in Deutschland zu fördern.